Cargando historial...
Modelos atómicos para estudiantes

Resumen de los modelos atómicos
| Modelo | Científico | Año | Características clave | Limitaciones |
|---|---|---|---|---|
| Dalton | John Dalton | 1803 | Esferas sólidas e indivisibles; los átomos del mismo elemento son idénticos | No explicaba la electricidad ni cómo se combinan los átomos |
| Thomson | J.J. Thomson | 1897 | Modelo del pudín de pasas; electrones incrustados en una esfera positiva | No explicaba la masa concentrada |
| Rutherford | Ernest Rutherford | 1911 | Núcleo con electrones orbitando; mayoritariamente espacio vacío | No explicaba la estabilidad de los electrones ni la energía |
| Bohr | Niels Bohr | 1913 | Electrones en órbitas circulares fijas a niveles de energía establecidos | Solo funcionaba para el hidrógeno; no coincidía con las observaciones |
| Schrödinger | Erwin Schrödinger | 1926 | Nubes de probabilidad de electrones (orbitales); dualidad onda-partícula | Matemáticas complejas; visualización abstracta |
El átomo: El bloque de construcción de todo
Los átomos son los bloques de construcción fundamentales de toda la materia del universo. Todo lo que puedes ver, tocar, oler o saborear está hecho de átomos: desde el aire que respiras hasta las estrellas del cielo. Comprender los átomos es la clave para entender la química, la física y la naturaleza de la realidad misma.
Una breve historia del descubrimiento atómico
Filosofía griega antigua (400 a. C.)
Demócrito y el "Atomos"
- Demócrito: Filósofo griego que propuso por primera vez la teoría atómica.
- "Atomos": Palabra griega que significa "indivisible".
- Idea básica: La materia no se puede dividir para siempre.
- Experimento mental: Cortar un trozo de materia repetidamente hasta que no se pueda cortar más.
La oposición de Aristóteles
- Aristóteles: Rechazó la teoría atómica.
- Cuatro elementos: En su lugar, propuso la tierra, el agua, el aire y el fuego.
- Materia continua: Creía que la materia era infinitamente divisible.
- Impacto: Las ideas de Aristóteles dominaron durante casi 2000 años.
Teoría atómica de John Dalton (1803)
El primer modelo atómico científico
- Base experimental: Basado en experimentos químicos y observaciones.
- Contribuciones clave: Hizo que la teoría atómica fuera científica en lugar de filosófica.
- Ley de las proporciones múltiples: Los elementos se combinan en proporciones de números enteros.
- Idea revolucionaria: Diferentes elementos tienen diferentes tipos de átomos.
Las ideas principales de Dalton
- Toda la materia está hecha de partículas diminutas e indivisibles llamadas átomos.
- Los átomos del mismo elemento son idénticos en masa y propiedades.
- Los átomos de diferentes elementos son diferentes.
- Los átomos se combinan en proporciones simples de números enteros para formar compuestos.
- Los átomos no se pueden crear, destruir ni transformar en otros átomos.
Lo que diferenciaba a Dalton de Demócrito:
- Basado en evidencia: Dalton utilizó datos experimentales, no solo filosofía.
- Cuantitativo: Asignó pesos relativos a diferentes átomos.
- Predictivo: Podía predecir cómo se combinarían los elementos.
- Comprobable: Otros científicos podían verificar sus conclusiones.
- Estudió las reacciones de los gases.
- Midió las proporciones de combinación de los elementos.
- Observó que los compuestos siempre tenían las mismas proporciones.
- Agua: siempre 8 partes de oxígeno por 1 parte de hidrógeno en masa.
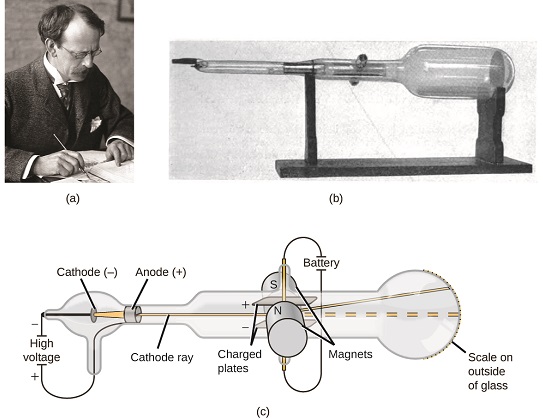
J.J. Thomson y el electrón (1897)
Los experimentos con rayos catódicos
- Rayos catódicos: Rayos misteriosos producidos en tubos de vacío.
- El descubrimiento de Thomson: Estos rayos eran flujos de partículas diminutas.
- Electrón: Primera partícula subatómica descubierta.
- Relación carga-masa: Thomson la midió con precisión.
El modelo del pudín de pasas
- Estructura: Los átomos son esferas de carga positiva.
- Electrones: Incrustados como pasas en un pudín (o pasas en un bizcocho).
- Distribuidos uniformeemente: Los electrones negativos se dispersan por todas partes.
- Información clave: Los átomos NO son indivisibles, ¡contienen partes!
Ernest Rutherford y el núcleo (1911)
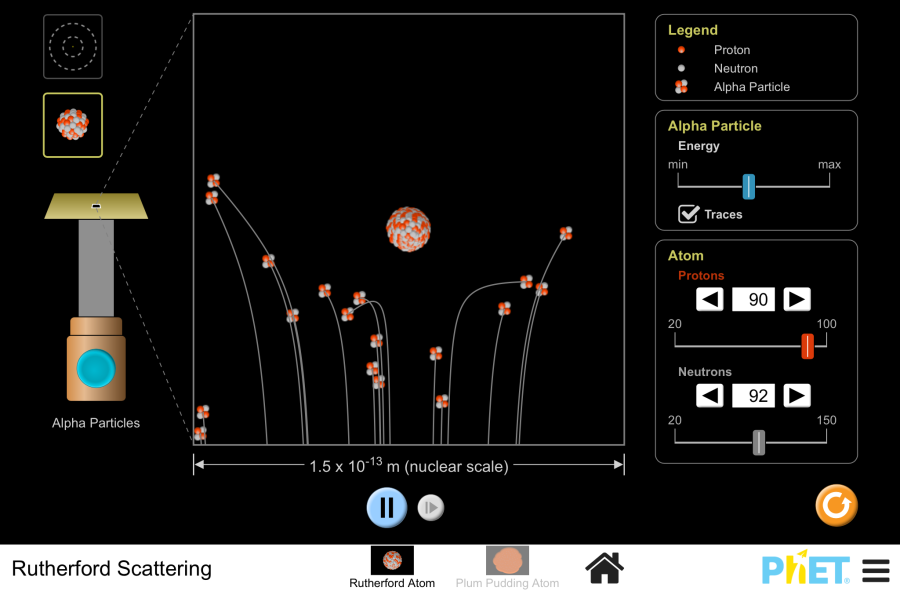
El experimento de la lámina de oro
- Configuración: Partículas alfa disparadas contra una fina lámina de oro.
- Resultado esperado: Todas las partículas pasan directamente (si el modelo del pudín de pasas fuera correcto).
- Resultado real: ¡La mayoría pasó, pero algunas rebotaron!
- La reacción de Rutherford: "Como si dispararas un cañón contra un pañuelo de papel y rebotara".
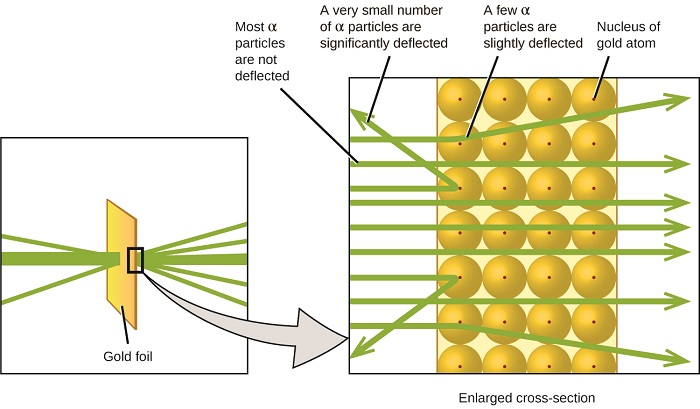
Descubrimiento del núcleo
- Conclusión: Los átomos tienen un centro positivo, pequeño y denso.
- El núcleo: Contiene la mayor parte de la masa del átomo.
- Espacio vacío: La mayor parte del átomo está vacío.
- Electrones: Orbitan lejos del núcleo.
Comprendiendo el experimento de Rutherford
- Partículas alfa (positivas) de una fuente radiactiva.
- Lámina de oro muy fina (solo unos pocos átomos de espesor).
- Pantalla fluorescente para detectar dónde aterrizan las partículas.
- Habitación oscura para observar destellos de luz.
- ~99% de las partículas pasaron directamente → los átomos están mayoritariamente vacíos.
- Algunas se desviaron en ángulos pequeños → cargas positivas que se repelen.
- ~1 de cada 8000 rebotó → golpeó algo muy denso y positivo.
- Tamaño del núcleo: unas 10.000 veces más pequeño que el átomo.
- Si el núcleo fuera una canica, el átomo sería un estadio de fútbol.
- Los electrones serían como moscas zumbando por el estadio.
El modelo de Niels Bohr (1913)
Niveles de energía cuantizados
- Problema con el modelo de Rutherford: Los electrones deberían caer en espiral hacia el núcleo.
- La solución de Bohr: Los electrones solo existen en órbitas específicas.
- Niveles de energía: Cada órbita tiene una energía fija.
- Saltos cuánticos: Los electrones saltan entre niveles, absorbiendo o emitiendo luz.
Características del modelo de Bohr
- Modelo planetario: Los electrones orbitan como planes alrededor del sol.
- Órbitas discretas: Solo se permiten ciertas distancias del núcleo.
- Emisión de energía: Se emite luz cuando los electrones bajan a niveles inferiores.
- Espectro del hidrógeno: Explicó con éxito las líneas espectrales del hidrógeno.
Modelo mecánico cuántico moderno (desde los años 20 hasta la actualidad)
Dualidad onda-partícula
- De Broglie: Propuso que los electrones se comportan como ondas.
- Schrödinger: Desarrolló la ecuación de onda para los electrones.
- Heisenberg: Principio de incertidumbre: no se puede conocer la posición y el momento exactos.
- Orbitales: Nubes de probabilidad donde es probable que existan los electrones.
Conceptos clave
- Sin órbitas fijas: Los electrones no siguen trayectorias específicas.
- Distribuciones de probabilidad: Solo podemos decir dónde es probable que estén los electrones.
- Nubes de electrones: Regiones de alta probabilidad de electrones.
- Formas complejas: Los orbitales s, p, d, f tienen diferentes geometrías.
¿Cómo "vemos" los átomos?
Dado que los átomos son increíblemente diminutos (alrededor de 10⁻¹⁰ metros, o una diezmilmillonésima de metro), no podemos verlos con microscopios ordinarios. Los científicos han desarrollado tecnologías asombrosas para visualizar estos diminutos bloques de construcción.
¿Por qué no podemos usar microscopios ordinarios?
El problema de la longitud de onda
- Límite de resolución: No se pueden ver objetos más pequeños que la longitud de onda utilizada.
- Longitud de onda de la luz visible: 400-700 nanómetros.
- Tamaño del átomo: Alrededor de 0,1-0,3 nanómetros.
- Conclusión: ¡Los átomos son ~1000 veces más pequeños que la longitud de onda de la luz!
Microscopía electrónica
Microscopio electrónico de transmisión (TEM)
- Desarrollado por: Ernst Ruska (años 30, Premio Nobel 1986).
- Principio: Utiliza haces de electrones en lugar de luz.
- Longitud de onda del electrón: Mucho más corta que la de la luz visible.
- Resolución: Puede ver átomos individuales en algunos materiales.
Microscopio electrónico de barrido (SEM)
- Principio: Escanea la superficie con un haz de electrones enfocado.
- Crea: Imágenes de superficies similares a 3D.
- Utilizado para: Análisis de la estructura de la superficie.
- Resolución: Muy alta, pero no llega al nivel atómico.
Microscopía de sonda de barrido
Microscopio de efecto túnel (STM)
- Inventado por: Gerd Binnig y Heinrich Rohrer (1981, Premio Nobel 1986).
- Principio: Utiliza el efecto túnel cuántico.
- Cómo funciona: Una aguja diminuta escanea muy cerca de la superficie.
- Resolución: ¡Puede obtener imágenes de átomos individuales!
- Imagen famosa: IBM escrito con 35 átomos de xenón (1989).
Microscopio de fuerza atómica (AFM)
- Principio: Una punta diminuta "siente" la superficie.
- Mide: Las fuerzas entre la punta y los átomos de la superficie.
- Ventajas: Funciona en materiales no conductores.
- Aplicaciones: Biología, ciencia de materiales, nanotecnología.
Cómo funciona el microscopio de efecto túnel
- Los electrones pueden "atravesar" barreras que clásicamente no deberían pasar.
- Se acerca una punta de metal afilada extremadamente cerca de una superficie (~1 nm).
- Los electrones pasan por efecto túnel entre la punta y la superficie.
- La corriente de túnel es extremadamente sensible a la distancia.
- La punta escanea la superficie siguiendo un patrón de barrido.
- El ordenador ajusta la altura de la punta para mantener la corriente constante.
- Los ajustes de altura mapean la topografía de la superficie.
- ¡Los átomos individuales aparecen como protuberancias en la imagen!
- Fue la primera vez que los humanos pudieron "ver" átomos individuales.
- También se puede usar para mover átomos individuales.
- Permitió la nanotecnología y la manipulación molecular.
Cristalografía de rayos X
Cómo funciona
- Principio: Los rayos X se difractan a través de las redes cristalinas.
- Análisis de patrones: El patrón de difracción revela la disposición atómica.
- Resolución: Puede determinar las posiciones atómicas con precisión.
- Uso famoso: Descubrimiento de la estructura del ADN (Watson, Crick, Franklin).
La escala de los átomos
Pequeñez increíble
- Diámetro del átomo: ~10⁻¹⁰ m (0,1 nanómetro).
- Diámetro del núcleo: ~10⁻¹⁵ m (¡100.000 veces más pequeño que el átomo!).
- Si el átomo fuera un estadio de fútbol: El núcleo sería un guisante en el centro.
Números asombrosos
- Átomos en un grano de arena: ~50.000.000.000.000.000.000 (5 × 10¹⁹).
- Átomos en el cuerpo humano: ~7 × 10²⁷.
- Átomos en una gota de agua: ~5 × 10²¹.
Mayoritariamente espacio vacío
- El núcleo contiene: El 99,9% de la masa del átomo.
- El núcleo ocupa: Solo 1/10.000.000.000.000 del volumen del átomo.
- Si quitaras todo el espacio vacío de los átomos: ¡Toda la raza humana cabría en un terrón de azúcar!
Puntos clave
- La teoría atómica evolucionó desde la filosofía griega hasta la mecánica cuántica moderna.
- Demócrito propuso los átomos por primera vez, pero Dalton lo hizo científico.
- Thomson descubrú los electrones y propuso el modelo del pudín de pasas.
- Rutherford descubrió el núcleo a través de su experimento de la lámina de oro.
- Bohr introdujo niveles de energía cuantizados para los electrones.
- Los átomos consisten en protones, neutrones (en el núcleo) y electrones (en la nube).
- Los protones determinan el elemento; los neutrones determinan el isótopo.
- Podemos "ver" los átomos usando microscopios electrónicos y microscopios de sonda de barrido.
- El STM puede obtener imágenes e incluso manipular átomos individuales.
- Los átomos son increíblemente diminutos: mayoritariamente espacio vacío con un núcleo denso.