Cargando historial...
| Propiedad | Metales 🧲 | Metaloides ⚗️ | No metales 🌬️ |
|---|---|---|---|
| Conductividad eléctrica | Alta | Media (semiconductores) | Baja |
| Conductividad térmica | Alta | Media | Baja |
| Apariencia | Brillante | Brillante o mate | Mate |
| Maleabilidad | Sí | No ## Hidrógeno |
El hidrógeno es verdaderamente único: el elemento más simple con solo un protón, pero alimenta las estrellas y ofrece la promesa de energía limpia para nuestro planeta. Como el elemento más abundante en el universo, el hidrógeno conecta la escala más pequeña de los átomos con la escala más grandiosa de las galaxias.
¿Qué hace que el hidrógeno sea especial?
El elemento más simple
Estructura básica
- Número atómico: 1 (un protón)
- Configuración electrónica: 1s¹ (un electrón)
- Masa atómica: 1,008 u (elemento más ligero)
- Símbolo: H (del griego "hydro" = agua, "genes" = creador)
Posición única
- Ubicación en la tabla periódica: A menudo se muestra por separado o en el Grupo 1.
- Ni metal ni no metal: Propiedades únicas.
- Puede perder o ganar electrones: Forma iones H⁺ y H⁻.
- Forma moléculas diatómicas: H₂ en la naturaleza.
Por qué el hidrógeno se comporta de forma tan única
Presencia universal
- Composición del universo: ~75% por masa, 90% por número de átomos.
- Estrellas: Combustible principal para la fusión nuclear.
- Espacio interestelar: Elemento más abundante.
- Big Bang: Primer elemento formado después del inicio del universo.
En la Tierra
- Corteza terrestre: 0,14% en peso.
- Forma combinada: Principalmente en el agua y compuestos orgánicos.
- Hidrógeno libre: Muy raro en la atmósfera (< 1 ppm).
- Importancia biológica: Componente esencial de todas las moléculas orgánicas.
Propiedades físicas
Estado gaseoso
Condiciones estándar
- Estado: Gas incoloro e inodoro.
- Densidad: 0,089 g/L (gas más ligero).
- Forma molecular: H₂ (diatómico).
- Fuerza del enlace: Enlace H-H muy fuerte (436 kJ/mol).
Condiciones extremas
- Punto de ebullición: -253 °C (-423 °F)
- Punto de fusión: -259 °C (-434 °F)
- Punto crítico: -240 °C, 13 atm.
- Hidrógeno líquido: Utilizado como combustible para cohetes.
Propiedades químicas
Reactividad
- Generalmente poco reactivo: Fuerte enlace H-H.
- Combustible: Arde en el aire con una llama casi invisible.
- Agente reductor: Puede eliminar el oxígeno de los compuestos.
- Forma compuestos: Con la mayoría de los elementos.
Comportamiento de los enlaces
- Enlace covalente: Comparte electrones con no metales.
- Carácter iónico: Puede formar iones H⁺ y H⁻.
- Enlace de hidrógeno: Atracción débil entre moléculas.
- Comportamiento metálico: Bajo presión extrema.
- No hay electrones internos que protejan la carga nuclear.
- Tamaño muy pequeño cuando forma H⁺.
- Puede acercarse mucho a otros núcleos.
- Forma enlaces muy fuertes en relación con su tamaño.
- Metales alcalinos: Tienen electrones internos, son mucho más grandes.
- Halógenos: Siete electrones, química diferente.
- Hidrógeno: Único - puede actuar como ambos.
- El H unido a N, O o F se vuelve parcialmente positivo.
- Atrae pares solitarios de otros átomos de N, O, F.
- Mucho más fuerte que las fuerzas de van der Waals.
- Crucial para la estructura del agua, el ADN y las proteínas.
- Forms very strong bonds relative to its size
- Alkali metals: Have inner electrons, much larger
- Halogens: Seven electrons, different chemistry
- Hydrogen: Unique - can act like both
- H bonded to N, O, or F becomes partially positive
- Attracts lone pairs on other N, O, F atoms
- Much stronger than van der Waals forces
- Crucial for water, DNA, protein structure
Metales
Los metales son elementos que pierden fácilmente electrones para formar iones positivos y se caracterizan por sus únicas propiedades físicas y químicas.
Posición en la tabla periódica
- Ubicación: Lado izquierdo y centro de la tabla periódica
- Grupos principales: Grupos 1, 2 y 13-15 (parcialmente)
- Metales de transición: Grupos 3-12
- Transición interna: Lantánidos y actínidos
Propiedades físicas clave de los metales
- Brillo: Superficies brillantes y reflectantes debido a los electrones móviles
- Conductividad eléctrica: Excelente; se utiliza en cableado (plata, cobre, aluminio)
- Conductividad térmica: Buena transferencia de calor; se utiliza en utensilios de cocina y radiadores
- Maleabilidad: Pueden martillearse en láminas (por ejemplo, lámina de oro, papel de aluminio)
- Ductilidad: Pueden estirarse en alambres (por ejemplo, cobre, oro)
- Dureza y resistencia: Varían ampliamente; la tendencia en cada período es que comienzan blandos y se endurecen en el medio de los metales de transición

Por qué los metales tienen estas propiedades únicas
- Los átomos metálicos pierden electrones de valencia
- Los iones positivos se disponen en un patrón regular
- Los electrones forman un "mar" alrededor de los iones positivos
- Los electrones están deslocalizados y son móviles
- Conductividad: Los electrones móviles transportan corriente y calor
- Brillo: Los electrones interactúan con la luz y la reflejan
- Maleabilidad/Ductilidad: El enlace no direccional permite que las capas se deslicen
- Resistencia: La atracción electrostática mantiene la estructura unida
- Compuestos iónicos: Electrones localizados, frágiles
- Compuestos covalentes: Enlaces direccionales, a menudo frágiles
- Metales: Combinación única de resistencia y flexibilidad
Una aleación es una mezcla de dos o más elementos, generalmente metales, creada para mejorar propiedades como la resistencia o la resistencia a la corrosión.
Ejemplos:- Bronce: Cobre + estaño (más duro y duradero que el cobre solo)
- Acero: Hierro + carbono (más resistente que el hierro puro)
- Latón: Cobre + zinc (se utiliza en instrumentos y accesorios)
Metaloides (Semimetales)
Los metaloides, también llamados semimetales, son los notables elementos que cierran la brecha entre los metales y los no metales. Estos elementos únicos impulsan nuestra era digital, desde el silicio en los chips de computadora hasta el boro en los materiales avanzados.
¿Qué son los metaloides?
Definición y características
Propiedades físicas
Apariencia
- Brillo: Brillo metálico o semimet álico
- Color: Variado - silicio (gris), boro (marrón), arsénico (gris)
- Fragilidad: Los metaloides sólidos son frágiles como los no metales
- Estructura cristalina: Formas cristalinas bien definidas
Propiedades eléctricas
- Comportamiento semiconductor: Característica clave
- Conductividad: Entre metales y no metales
- Dependencia de la temperatura: La conductividad aumenta con la temperatura
- Sensibilidad a la pureza: Las pequeñas impurezas afectan mucho la conductividad
La importancia de los semiconductores
Los semiconductores son materiales con conductividad entre metales y aislantes, cruciales para la electrónica. Su conductividad se puede controlar con precisión agregando pequeñas cantidades de otros elementos (dopaje).
Tipo n: Dopado con elementos como el fósforo (electrones extra, portadores de carga negativa) Tipo p: Dopado con elementos como el boro (crea "huecos", portadores de carga positiva) Uniones p-n (donde el tipo n y el tipo p se encuentran) permiten que la corriente fluya en una dirección, clave para diodos, transistores y células solares.Propiedades de los semiconductores
¿Qué son los semiconductores?
No metales
Los no metales son elementos esenciales que componen el aire que respiramos, el agua que bebemos y las moléculas orgánicas en nuestros cuerpos. A pesar de ser menos numerosos que los metales, los no metales desempeñan papeles cruciales en la química, la biología y la tecnología.
Hay una enorme variedad de no metales, desde los gases que llenan nuestra atmósfera hasta los sólidos que forman la base de la vida. Se definen por su tendencia a ganar electrones y formar iones negativos, así como su alta electronegatividad y capacidad para formar enlaces covalentes.
Posición en la tabla periódica
- Ubicación: Área superior derecha de la tabla periódica
- Grupos: Principalmente grupos 14-18
Propiedades físicas de los no metales
Pobre conductividad eléctrica
- Razón: Los electrones están bloqueados en enlaces covalentes
- Excepción: El grafito (carbono) conduce la electricidad porque crean electrones π deslocalizados
Pobre conductividad térmica
Fragilidad
- No metales sólidos: Se rompen en lugar de doblarse
Apariencia
- Apariencia: Opaca, sin brillo
- Colores: Variados - azufre amarillo, bromo rojo, yodo púrpura
Estados de la materia
- Variedad: Pueden ser gases, líquidos o sólidos a temperatura ambiente
- Compuestos pequeños: A menudo gases (O₂, N₂)
- Moléculas más grandes: A menudo sólidos (azufre, fósforo, diamantes)
Alótropos
Los alótropos son diferentes formas estructurales del mismo elemento, con propiedades físicas y químicas distintas. Por ejemplo, el carbono tiene varios alótropos, incluyendo el diamante (duro, aislante), el grafito (blando, conductor), los fullerenos (moléculas esféricas) y el grafeno (capa única de átomos de carbono).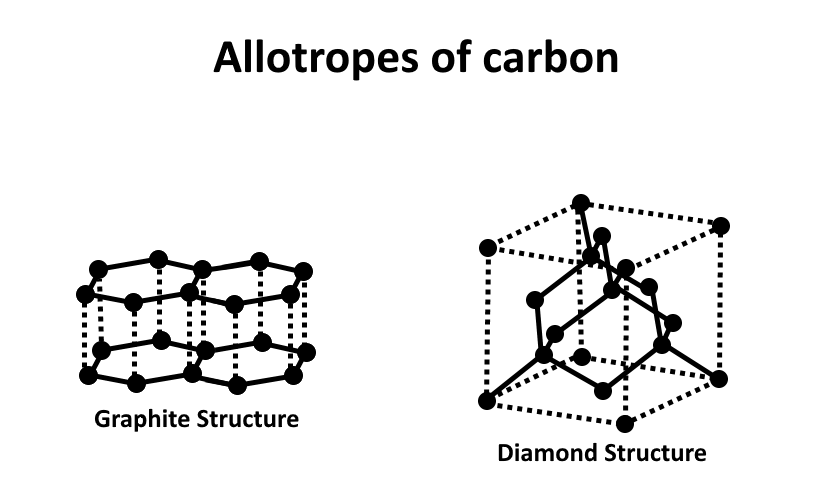
Gases nobles
Son los elementos inertes y nobles del Grupo 18, con capas externas de electrones completas que los hacen estables e inertes. A pesar de su falta de reactividad, los gases nobles tienen importantes aplicaciones en iluminación, soldadura e incluso en mezclas de gases para el buceo en profundidad.
Uso:
- Protegen las cosas de reacciones (como el caso del argón en bombillas)
- Iluminación: Letreros de neón, argón en bombillas incandescentes, xenón en lámparas de alta intensidad
- Enfriamiento: Helio líquido para imanes superconductores, nitrógeno líquido para criogenia