Cargando historial...
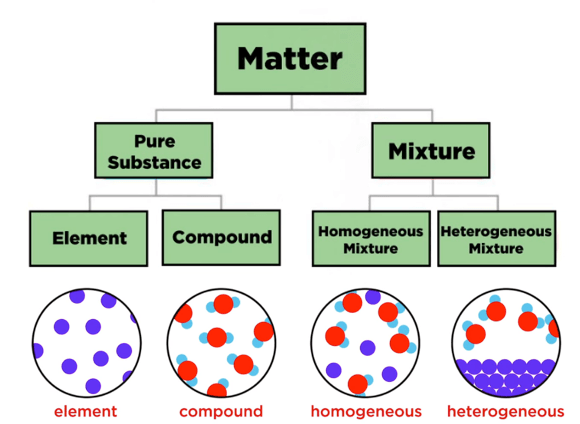
Todo lo que nos rodea está hecho de materia, y la materia se organiza en elementos y compuestos. Comprender estos bloques básicos nos ayuda a explicar cómo funciona el mundo a escala atómica.
¿Qué son los elementos?
Definición y características
Un elemento es una sustancia pura formada por un solo tipo de átomo y que no puede descomponerse en sustancias más simples mediante procesos químicos.
Propiedades clave de los elementos
- Sustancias puras: Formadas por un único tipo de átomo
- No se descomponen químicamente: No pueden separarse en sustancias más simples por reacciones químicas habituales
- Identidad única: Cada elemento tiene un número atómico propio
- Propiedades características: Cada uno presenta propiedades físicas y químicas específicas
- Bloques de construcción: Se combinan para formar otras sustancias
¿Qué son los compuestos?
Definición y formación
Un compuesto es una sustancia pura formada cuando dos o más elementos diferentes se unen químicamente en proporciones fijas.
Los compuestos suelen estar formados por moléculas, que son las unidades más pequeñas que conservan sus propiedades. Por ejemplo, una molécula de agua (H₂O) contiene dos átomos de hidrógeno y uno de oxígeno unidos entre sí.
Propiedades clave de los compuestos
- Varios elementos: Contienen siempre dos o más elementos distintos
- Enlaces químicos: Los átomos están unidos por fuerzas químicas
- Composición fija: Mantienen siempre la misma proporción de elementos
- Nuevas propiedades: Sus propiedades son diferentes de las de los elementos por separado
- Pueden descomponerse: Se pueden separar por métodos químicos
Fórmulas químicas
Los compuestos se representan mediante fórmulas químicas que indican:
- Símbolos químicos: Qué elementos están presentes
- Subíndices: Cuántos átomos hay de cada elemento
- Proporciones: Relación fija entre los elementos
Lectura de fórmulas químicas
- H₂O: 2 átomos de hidrógeno + 1 de oxígeno = agua
- CO₂: 1 átomo de carbono + 2 de oxígeno = dióxido de carbono
- NaCl: 1 átomo de sodio + 1 de cloro = sal de mesa
- C₆H₁₂O₆: 6 de carbono + 12 de hidrógeno + 6 de oxígeno = glucosa
Comparación entre elementos y compuestos
| Propiedad | Elementos | Compuestos |
|---|---|---|
| Composición | Un solo tipo de átomo | Dos o más elementos diferentes |
| Separación | No se descomponen químicamente | Pueden descomponerse en elementos |
| Propiedades | Propias de cada elemento | Diferentes a las de sus elementos constituyentes |
| Ejemplos | H, O, C, Fe, Au | H₂O, CO₂, NaCl, C₆H₁₂O₆ |
| Formación | No se obtienen a partir de sustancias más simples | Se forman por combinación química de elementos |
| Símbolos/Fórmulas | Símbolo de un elemento (ej., O) | Fórmula química (ej., H₂O) |