Cargando historial...
Partículas subatómicas y cálculos atómicos
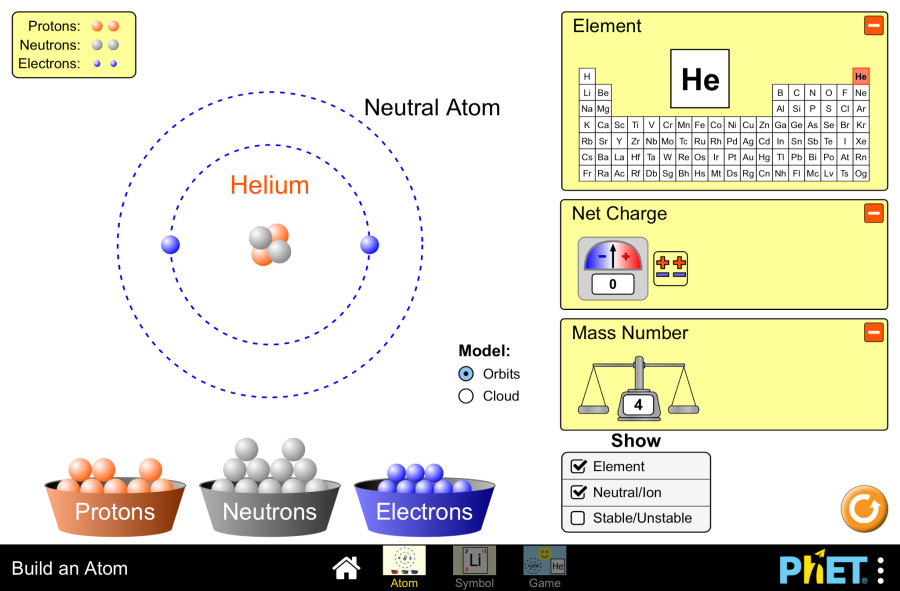
Las tres partículas subatómicas
| Partícula | Símbolo | Carga | Masa (u) | Masa (kg) | Ubicación |
|---|---|---|---|---|---|
| Protón | p | +1 | 1 | 1.673 × 10⁻²⁷ | Núcleo |
| Neutrón | n | 0 | 1 | 1.675 × 10⁻²⁷ | Núcleo |
| Electrón | e | -1 | ≈ 0 | 9.109 × 10⁻³¹ | Nube electrónica |
Fórmulas clave

| Símbolo | Nombre | Fórmula |
|---|---|---|
| Z | Número atómico | = número de protones |
| A | Número másico | = protones + neutrones |
| n | Neutrones | = A - Z |
| e | Electrones (átomo neutro) | = protones |
| Carga | Carga del ion | = protones - electrones |
Ejemplos resueltos
Ejemplo 1: Átomo neutro — ¹⁶₈O (Oxígeno-16)
| Símbolo | Valor | ¿Cómo? |
|---|---|---|
| Z | 8 | Dado (número inferior) |
| A | 16 | Dado (número superior) |
| p | 8 | p = Z |
| n | 8 | n = A - Z = 16 - 8 |
| e | 8 | e = p (neutro) |
| Carga | 0 | Átomo neutro |
Ejemplo 2: Catión (+) — ²³₁₁Na⁺ (ion sodio)
| Símbolo | Valor | ¿Cómo? |
|---|---|---|
| Z | 11 | Dado |
| A | 23 | Dado |
| p | 11 | p = Z |
| n | 12 | n = A - Z = 23 - 11 |
| e | 10 | Pierde 1 electrón |
| Carga | +1 | p - e = 11 - 10 |
Ejemplo 3: Anión (-) — ³²₁₆S²⁻ (ion sulfuro)
| Símbolo | Valor | ¿Cómo? |
|---|---|---|
| Z | 16 | Dado |
| A | 32 | Dado |
| p | 16 | p = Z |
| n | 16 | n = A - Z = 32 - 16 |
| e | 18 | Gana 2 electrones |
| Carga | -2 | p - e = 16 - 18 |
Ejemplo 4: Identificar a partir de partículas — p = 26, n = 30, e = 24
| Símbolo | Valor | ¿Cómo? |
|---|---|---|
| p | 26 | Dado |
| Z | 26 | Z = p |
| Elemento | Hierro (Fe) | Buscar Z = 26 |
| n | 30 | Dado |
| A | 56 | A = p + n = 26 + 30 |
| e | 24 | Dado |
| Carga | +2 | p - e = 26 - 24 |
| Ión | Fe²⁺ | Catión (pierde 2 e) |
Tablas de práctica
Tabla 1: Átomos neutros
Completa los valores que faltan:
| Elemento | Símbolo | Z | A | p | n | e | Carga |
|---|---|---|---|---|---|---|---|
| Hidrógeno | ¹₁H | 1 | 1 | 1 | 0 | 1 | 0 |
| Carbono | ¹²₆C | 6 | 12 | 6 | 6 | 6 | 0 |
| Nitrógeno | ¹⁴₇N | 7 | 14 | 7 | 7 | 7 | 0 |
| Oxígeno | ¹⁶₈O | 8 | 16 | 8 | 8 | 8 | 0 |
| Sodio | ²³₁₁Na | 11 | 23 | 11 | 12 | 11 | 0 |
| Cloro | ³⁵₁₇Cl | 17 | 35 | 17 | 18 | 17 | 0 |
| Hierro | ⁵⁶₂₆Fe | 26 | 56 | 26 | 30 | 26 | 0 |
Tabla 2: Cationes (iones positivos)
| Ión | Z | A | p | n | e | Carga |
|---|---|---|---|---|---|---|
| Na⁺ | 11 | 23 | 11 | 12 | 10 | +1 |
| K⁺ | 19 | 39 | 19 | 20 | 18 | +1 |
| Mg²⁺ | 12 | 24 | 12 | 12 | 10 | +2 |
| Ca²⁺ | 20 | 40 | 20 | 20 | 18 | +2 |
| Al³⁺ | 13 | 27 | 13 | 14 | 10 | +3 |
| Fe²⁺ | 26 | 56 | 26 | 30 | 24 | +2 |
| Fe³⁺ | 26 | 56 | 26 | 30 | 23 | +3 |
| Cu²⁺ | 29 | 64 | 29 | 35 | 27 | +2 |
Tabla 3: Aniones (iones negativos)
| Ión | Z | A | p | n | e | Carga |
|---|---|---|---|---|---|---|
| F⁻ | 9 | 19 | 9 | 10 | 10 | -1 |
| Cl⁻ | 17 | 35 | 17 | 18 | 18 | -1 |
| Br⁻ | 35 | 80 | 35 | 45 | 36 | -1 |
| O²⁻ | 8 | 16 | 8 | 8 | 10 | -2 |
| S²⁻ | 16 | 32 | 16 | 16 | 18 | -2 |
| N³⁻ | 7 | 14 | 7 | 7 | 10 | -3 |
| P³⁻ | 15 | 31 | 15 | 16 | 18 | -3 |
Isótopos
Isótopos = mismo Z (protones), distinto n (neutrones)Isótopos del hidrógeno
| Nombre | Símbolo | Z | A | p | n | e | Abundancia | Estabilidad | Uso / presencia |
|---|---|---|---|---|---|---|---|---|---|
| Protio | ¹₁H | 1 | 1 | 1 | 0 | 1 | 99.98% | Estable | El más común; presente en el agua (H₂O) y en compuestos orgánicos |
| Deuterio | ²₁H (D) | 1 | 2 | 1 | 1 | 1 | 0.02% | Estable | Agua pesada (D₂O) en reactores nucleares; espectroscopía RMN |
| Tritio | ³₁H (T) | 1 | 3 | 1 | 2 | 1 | Traza | ☢️ Radiactivo (t½ = 12.3 a) | Combustible de fusión nuclear; relojes luminiscentes; se produce en reactores nucleares |
Isótopos del carbono
| Nombre | Símbolo | Z | A | p | n | e | Abundancia | Estabilidad | Uso / presencia |
|---|---|---|---|---|---|---|---|---|---|
| Carbono-12 | ¹²₆C | 6 | 12 | 6 | 6 | 6 | 98.9% | Estable | Referencia de la unidad de masa atómica (1 u = 1/12 de ¹²C); materia orgánica |
| Carbono-13 | ¹³₆C | 6 | 13 | 6 | 7 | 6 | 1.1% | Estable | Espectroscopía RMN; estudios metabólicos; investigación climática |
| Carbono-14 | ¹⁴₆C | 6 | 14 | 6 | 8 | 6 | Traza | ☢️ Radiactivo (t½ = 5,730 a) | Datación por radiocarbono de fósiles y restos arqueológicos; se forma en la atmósfera por rayos cósmicos |
Gráfico de estabilidad nuclear
Identifica el elemento
Usa la tabla periódica para identificar elementos a partir de sus datos:
Tabla 4: Encuentra el elemento
| Z | A | p | n | e | Carga | Elemento | Isótopo | Símbolo |
|---|---|---|---|---|---|---|---|---|
| 1 | 1 | 1 | 0 | 1 | 0 | Hidrógeno | Protio | 1H |
| 6 | 12 | 6 | 6 | 6 | 0 | Carbono | Carbono-12 | 12C |
| 8 | 16 | 8 | 8 | 10 | -2 | Oxígeno | Oxígeno-16 | 16O2- |
| 11 | 23 | 11 | 12 | 10 | +1 | Sodio | Sodio-23 | 23Na+ |
| 17 | 35 | 17 | 18 | 18 | -1 | Cloro | Cloro-35 | 35Cl- |
| 26 | 56 | 26 | 30 | 24 | +2 | Hierro | Hierro-56 | 56Fe2+ |
| 20 | 40 | 20 | 20 | 18 | +2 | Calcio | Calcio-40 | 40Ca2+ |