Cargando historial...
¿Qué es el calor?
El calor es la transferencia de energía térmica entre objetos debido a una diferencia de temperatura. Siempre fluye del objeto caliente al frío hasta que se alcanza el equilibrio térmico (igual temperatura).
1. Mecanismos de transferencia de calor
El calor puede moverse de tres maneras:
| Mecanismo | Idea principal | Medio |
|---|---|---|
| Conducción | Contacto directo | Sólidos (principalmente) |
| Convección | Movimiento de fluidos | Líquidos y Gases |
| Radiación | Ondas | Vacío y medios transparentes |
A. Conducción
Transferencia a través del contacto directo donde las partículas vibran y pasan energía a sus vecinas. Los metales son excelentes conductores porque tienen "electrones libres" que mueven la energía rápidamente.Curiosidades y ejemplos de conducción
- Conductividad térmica (k): Un valor que mide qué tan rápido se mueve el calor. El cobre (k=400) es mucho más rápido que la madera (k=0,1).
- La cuchara "fría": Una cuchara de metal se siente más fría que una de madera incluso si ambas están a 20°C porque el metal aleja el calor de tu mano más rápido.
- Doble acristalamiento: Las ventanas utilizan una capa de aire entre dos paneles de vidrio. Como el aire es un pésimo conductor, mantiene la casa caliente.
B. Convección
Transferencia a través del movimiento real de un fluido (líquido o gas). El fluido caliente se expande, se vuelve menos denso y asciende, mientras que el fluido frío desciende. Esto crea corrientes de convección.Curiosidades y ejemplos de convección
- Brisas marinas: Durante el día, la tierra se calienta más rápido que el mar. El aire caliente sobre la tierra asciende y el aire fresco del mar sopla para reemplazarlo.
- Radiadores: Generalmente se colocan en la parte inferior de una habitación para que el aire caliente pueda subir y circular de forma natural.
- Agua hirviendo: Puedes ver "corrientes" en una olla mientras el agua caliente del fondo se mueve hacia arriba.
C. Radiación
Transferencia a través de ondas electromagnéticas (principalmente infrarrojas). Es la única forma en que el calor puede viajar a través del vacío (como el espacio).Curiosidades y ejemplos de radiación
- El Sol: Sentimos el calor del Sol a pesar de que hay 150 millones de kilómetros de espacio vacío entre nosotros.
- Colores: Las superficies negras absorben la radiación (y se calientan), mientras que las superficies blancas/brillantes la reflejan.
- Visión nocturna: Las cámaras térmicas "ven" la radiación infrarroja emitida por cuerpos calientes como humanos o animales.
2. Calor específico
Para calcular la cantidad de energía (calor) necesaria para cambiar la temperatura de un objeto, utilizamos la siguiente fórmula:
- Q = Energía térmica transferida (Julios, J)
- m = Masa de la sustancia (kg)
- c_e = Calor específico (J/kg·°C)
- ΔT = Cambio de temperatura (\(T_{final} - T_{inicial}\))
Calor específico (\(c_e\))
Es la energía necesaria para elevar la temperatura de 1 kg de una sustancia en 1°C.| Material | \(c_e\) (J/kg·°C) | ¿Por qué es importante? |
|---|---|---|
| Agua | 4.200 | ¡Muy alto! Los océanos se mantienen frescos en verano. |
| Hielo | 2.100 | La mitad que el agua líquida. |
| Aluminio | 900 | Bueno para sartenes. |
| Vidrio | 840 | Aislante promedio. |
| Hierro | 450 | Se calienta rápidamente. |
| Plomo | 130 | Se calienta extremadamente rápido. |
Ejemplos resueltos
Ejemplo 1: ¿Cuánto calor se necesita para calentar 2 kg de agua de 20°C a 50°C? (\(c_e = 4.200\) J/kg·°C)
- Identificar datos: m = 2 kg, \(c_e = 4.200\), ΔT = 50 - 20 = 30°C
- Aplicar fórmula: \(Q = 2 \times 4.200 \times 30\)
- Resultado: \(Q = 252.000 \text{ J}\)
Ejemplo 2: Una barra de hierro de 0,5 kg se enfría de 100°C a 20°C. ¿Cuánto calor libera? (\(c_e = 450\) J/kg·°C)
- Identificar datos: m = 0,5 kg, \(c_e = 450\), ΔT = 20 - 100 = -80°C
- Aplicar fórmula: \(Q = 0,5 \times 450 \times (-80)\)
- Resultado: \(Q = -18.000 \text{ J}\) (El signo negativo significa que la energía se pierde/libera)
3. Calor latente (cambios de fase)
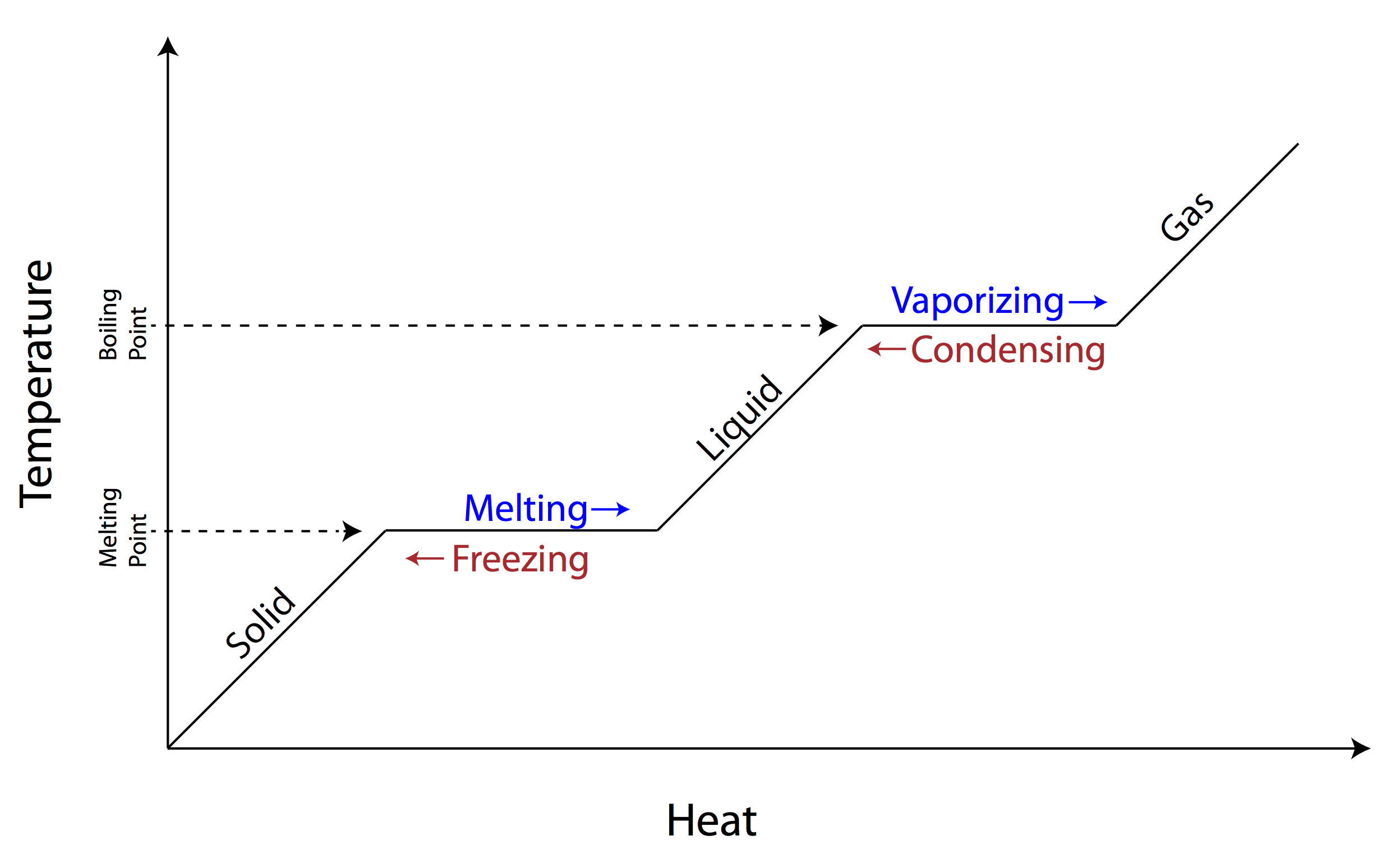
Cuando una sustancia cambia de estado (como el hielo derritiéndose), absorbe calor sin cambiar su temperatura.
- L = Calor latente (J/kg). Para la fusión del agua (derretimiento), \(L = 334.000 \text{ J/kg}\).
Ejemplo 3: ¿Cuánto calor se necesita para derretir 2 kg de hielo a 0°C? (\(L = 334.000\) J/kg)
- Identificar datos: m = 2 kg, \(L = 334.000\)
- Aplicar fórmula: \(Q = 2 \times 334.000\)
- Resultado: \(Q = 668.000 \text{ J}\)
4. Cálculos combinados (varios pasos)
Cuando una sustancia debe calentarse hasta su punto de fusión antes de poder derretirse, o calentarse más después de derretirse, sumamos el calor de cada paso.
Ejemplo 4: Calcula el calor necesario para convertir 1 kg de hielo a -10°C en agua a 0°C (\(c_{hielo} = 2.100\), \(L_{fusión} = 334.000\)).
- Paso 1: Calentar el hielo hasta 0°C
- Paso 2: Derretir el hielo a 0°C
- Total: \(Q_1 + Q_2 = 21.000 + 334.000 = \textbf{355.000 J}\)
Ejemplo 5: ¿Cuánto calor se necesita para convertir 0,2 kg de hielo a -10°C en agua a 50°C?
- Paso 1: Calentar hielo a 0°C: \(Q_1 = 0,2 \times 2.100 \times 10 = 4.200 \text{ J}\)
- Paso 2: Derretir hielo a 0°C: \(Q_2 = 0,2 \times 334.000 = 66.800 \text{ J}\)
- Paso 3: Calentar agua a 50°C: \(Q_3 = 0,2 \times 4.200 \times 50 = 42.000 \text{ J}\)
- Total: \(4.200 + 66.800 + 42.000 = \textbf{113.000 J}\)
4. Leyes de la termodinámica
| Ley | Enunciado | Ejemplo |
|---|---|---|
| Ley Cero | Los sistemas tienden a alcanzar el equilibrio térmico | Dos cuerpos a diferentes temperaturas en contacto terminan a la misma temperatura |
| 1ª Ley | La energía se conserva: puede transformarse pero nunca crearse ni destruirse | La energía química del combustible se convierte en calor y energía mecánica en un motor |
| 2ª Ley | La energía tiende a dispersarse y volverse menos útil (la entropía aumenta) | El calor fluye naturalmente de caliente a frío, nunca al revés por sí solo |