Cargando historial...
Termodinamica quimica
La termodinamica quimica estudia los intercambios de energia en las reacciones.
Reacciones exotermicas
Una reaccion exotermica libera energia al entorno:
- El entorno se calienta.
- Los productos quedan con menor energia que los reactivos.
- ΔH es negativo (ΔH < 0).
Ejemplos: combustion, respiracion celular, neutralizacion acido-base.
Reacciones endotermicas
Una reaccion endotermica absorbe energia del entorno:
- El entorno se enfria.
- Los productos quedan con mayor energia que los reactivos.
- ΔH es positivo (ΔH > 0).
Ejemplos: fotosintesis, descomposicion termica, bolsas frias instantaneas.
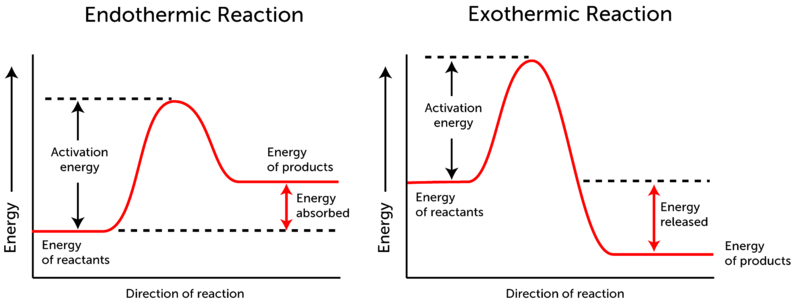
Diagramas de energia
Un diagrama de energia muestra:
- Eje y: energia potencial.
- Eje x: avance de la reaccion.
- Energia de activacion (\(E_a\)): barrera minima para iniciar la reaccion.
En exotermicas, el nivel final es menor que el inicial. En endotermicas, el nivel final es mayor.